
[Índice] [Introducción] [Matriz] [Osteoblasto] [Osteoclasto] [Biomecanica] [Dinamica] [Bibliografía] |
El esqueleto , a pesar de estar constituido en su mayor parte por matriz extracelular, es uno de los sistemas más dinámicos del organismo y presenta fenómenos de crecimiento, modelado, remodelado y reparación.
El crecimiento óseo se inicia en la vida embrionaria y sigue hasta la pubertad. El crecimiento en longitud se efectúa mediante la adición de hueso nuevo a la cara diafisaria de la placa de crecimiento o fisis2.
La placa de crecimiento es una estructura con forma de disco que se halla intercalada entre la epífisis y la diáfisis. En la placa de crecimiento se distinguen dos regiones, una central y otra periférica. La región central está constituida por cartílago hialino en el que se distinguen, desde la epífisis a la diáfisis, cuatro zonas: zona germinal, zona proliferativa, zona de cartílago hipertrófico y zona de cartílago calcificado2.
Zona germinal (capa de reserva o de reposo): Es la zona más cercana a la epífisis. Está constituida por células cartilaginosas aisladas de forma oval. En esta capa se observan mitosis y existe una intensa síntesis de matriz extracelular
Zona proliferativa: Se halla constituida por células cartilaginosas en forma de cuńa cuyo eje mayor es perpendicular al del hueso. Estas células se disponen en columnas paralelas al eje longitudinal del hueso. En esta zona también se observan mitosis y existe una intensa síntesis de matriz extracelular. Las células de cada columna parecen dividirse al unísono pero de manera asicrónica con respecto a las de las columnas restantes.
Zona de cartílago hipertrófico: Los condrocitos de esta zona maduran, adquieren forma redondeada y su tamańo aumenta a medida que se alejan de la epífisis.
Zona de cartílago calcificado: En esta zona la matriz cartilaginosa se mineraliza. El núcleo de los condrocitos pierde cromatina (cariolisis) y su citoplasma se vacuoliza. Finalmente estas células mueren y desaparecen por lo que en el extremo de cada columna se observa un espacio vacio rodeado por matriz cartilaginosa calcificada que corresponde al que anteriormente ocupaba un condrocito. Sobre esta matriz calcificada los osteoblastos del estroma de la medula diafisaria depositarán hueso plexiforme (osificación de tipo endocondral). En el curso del modelado óseo este hueso inmaduro será sustituido por hueso laminar.
La región periférica de la placa de crecimiento se denomina zona de Ranvier. Esta zona es un anillo de sección triangular y base externa que rodea la región central de la fisis. La zona de Ranvier se halla constituida por células inmaduras con diferenciación condroblástica y osteoblástica. Las primeras podrían contribuir al crecimiento circunferencial de la placa de crecimiento y las segundas podrían contribuir al crecimiento en longitud de la cortical diafisaria.
El crecimiento en espesor del hueso se logra mediante la aposición concéntrica subperióstica de tejido óseo. Las células de la capa mas interna del periostio se diferencian en osteoblastos que depositan hueso directamente sobre la superficie externa de la cortical diafisaria (osificación de tipo intramembranoso).
El crecimiento oseo22 depende de factores genéticos y se halla influido por factores sistémicos (hormonas) y locales. Las hormonas que intervienen en el control del crecimiento óseo se pueden dividir en cuatro grupos:
- Hormonas necesarias para el crecimiento: hormona de crecimiento, hormona tiroidea, insulina.
- Hormonas inhibidoras del crecimiento: cortisol
- Hormonas activadoras de la maduración: hormonas sexuales
- Vitamina D y Hormona paratiroidea
Los factores locales que pueden influir sobre el crecimiento son de tipo nervioso y de tipo mecánico. Se desconoce el mecanismo por el que el sistema nervioso interviene sobre el crecimiento óseo. Se ha sugerido que podría intervenir de manera indirecta a través del control del flujo sanguineo. El resultado de la acción de las fuerzas mecánicas depende de su intensidad así como de su dirección y sentido. Las fuerzas de compresión paralelas a la dirección del crecimiento disminuyen la actividad de la fisis. Las fuerzas de tracción paralelas a la dirección del crecimiento si son de pequeńa intensidad pueden incrementar ligeramente el crecimiento pero si son de gran magnitud pueden causar epifisiolisis ó fusión prematura. Las fuerzas perpendiculares a la dirección del crecimiento producen un efecto deformante que es directamente proporcional a la fuerza aplicada e inversamente proporcional al diámetro del hueso.
En las metáfisis22, el crecimiento óseo se asocia a fenómenos de reabsorción en la superficie externa y de formación en la interna, mientras que, en las diáfisis, ocurre lo contrario. Este proceso se denomina modelado óseo y permite que los distintos huesos conserven su forma durante el proceso de crecimiento. Asimismo el modelado óseo es el mecanismo que permite una renovación constante del esqueleto antes de que cese el crecimiento Las alteraciones del modelado pueden causar deformidades óseas.
El modelado esta programado geneticamente pero es probable que existan factores mecánicos de carácter local que pueden influir sobre el mismo. En este sentido existen datos experimentales que sugieren que la tensión que ejerce el manguito perióstico sobre ambos extremos óseos es un factor que contribuye a que aparezcan osteoclastos sobre la superficie externa del cono metafisario23.
En el adulto, cerca de un 8% del tejido óseo es renovado anualmente. Esta cifra es superior en el joven e inferior en el anciano24. El remodelado óseo se lleva a cabo mediante la acción sucesiva (acoplamiento) de osteoclastos y osteoblastos sobre una misma superficie ósea. Cada ciclo de remodelado consta de tres fases: reabsorción, reposo o inversión y formación. En la fase de reabsorción, un grupo de osteoclastos se diferencia a partir de sus precursores y erosiona una superficie ósea dando lugar a imágenes en sacabocados conocidas como lagunas de Howship (John Howship, 1781-1841)24. Una vez finalizada la reabsorción los osteoclastos son eliminados por apoptosis. La fase de reposo o inversión es un periodo de aparente inactividad. Durante la fase de formación un grupo de osteoblastos se diferencia a partir de sus precursores y rellena con hueso nuevo la zona excavada por los osteoclastos. Los osteoblastos depositan en primer lugar matriz ósea no mineralizada que forma una capa de unas 10 micras de espesor denominada ribete de osteoide (Fig.3). Entre el deposito de osteoide y su mineralización existe un tiempo de demora de unos 10 a 20 días (Mineral Lag Time)24. Durante este periodo la matriz ósea sufre cambios en su composición y estructura que la hacen apta para el deposito de mineral (maduración de la matriz). La mineralización se inicia en la interfase entre el osteoide y el hueso mineralizado preexistente y avanza hacia la superficie a lo largo de un plano de barrido de 2 a 3 micras de espesor. Este plano, integrado en parte por mineral amorfo, se denomina frente de mineralización24 (Fig.11). A medida que este frente se desplaza va dejando tras de sí matriz ósea mineralizada en forma de cristales de hidroxiapatita (fig.3). Una vez completado el depósito de hueso los osteoblastos que no se han incorporado a la matriz se aplanan y pasan a formar parte del endostio (lining cells).
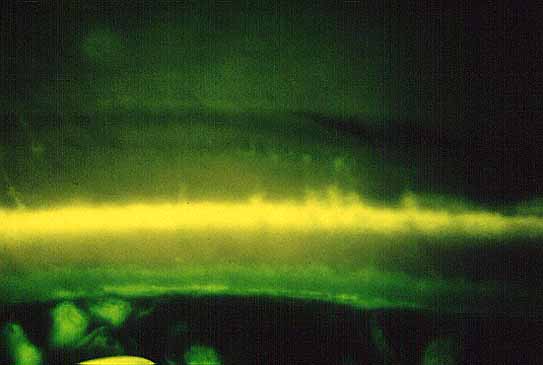 |
Fig.11: El frente de mineralización aparece como una linea fluorescente de color amarillo (Marcaje in vivo con tetraciclinas x 400). |
El conjunto de osteoclastos y osteoblastos que de manera coordinada actúan en una superficie ósea durante un ciclo de remodelado recibe el nombre de Unidad Multicelular Básica (Basic Multicellular Unit: BMU)25. Las BMU se activan de manera asincrónica, por lo que mientras unos ciclos de remodelado se hallan en fase de reabsorción, otros se encuentran en fase de reposo o de formación. El nuevo segmento de tejido óseo que resulta de la acción de cada BMU se denomina Unidad Estructural Osea (Bone Structural Unit: BSU). El límite entre el hueso preexistente y la nueva BSU es identificable morfológicamente como una línea ondulada y recibe el nombre de superficie de inversión o de cemento2 (Fig.12). En la remodelación del hueso compacto los osteoclastos, partiendo de un canal de Havers o de Volkmann, excavan un túnel de sección circular. Por esta razón las BSU corticales, llamadas también osteonas2, tienen forma cilíndrica (Fig.12). En la remodelación del hueso esponjoso los osteoclastos labran, en la superficie de las trabéculas, excavaciones poco profundas y de base ancha (Fig.12). Por esta razón las BSU trabeculares llamadas también paquetes trabeculares tienen forma de lente plano-convexa.
Se denomina recambio óseo (bone turnover) al volumen total de hueso que es renovado por unidad de tiempo mediante el remodelado24. El recambio óseo es directamente proporcional al número de ciclos de remodelado en curso o, lo que es lo mismo, al número de BMU activas. La diferencia entre el volumen de hueso formado y el de hueso reabsorbido, por unidad de tiempo, se denomina balance óseo24. Si la reabsorción y la formación son idénticas, el balance es igual a cero y el volumen total de hueso (masa ósea) no variará en función del tiempo. Si la formación y la reabsorción no son iguales, la masa ósea se modificará en sentido positivo o negativo. El balance óseo corresponde a la suma aritmética del hueso ganado o perdido en cada ciclo de remodelado. Así pues, una vez instaurado un balance positivo o negativo la velocidad a la que se perderá o ganará masa ósea será directamente proporcional al número de BMU activas. La máxima masa ósea se alcanza a los 30 ańos de edad y depende de factores genéticos (gen del receptor de la vitamina D) y ambientales (ingesta de calcio, ejercicio físico). De los 30 a los 40 ańos el balance óseo es igual a cero y la masa ósea permanece estable. A partir de los 40 ańos se instaura un balance negativo y la masa ósea disminuye de manera progresiva. En el hombre, la pérdida se realiza a una velocidad constante (un 0,5% anual) mientras que en la mujer se acelera durante los ańos de la menopausia. Esta pérdida "fisiológica" de masa ósea determina que al inicio de la octava década los hombres hayan disminuido su masa ósea en un 20% y las mujeres en un 30%.
El remodelado óseo está sometido a un control sistémico (hormonas) y a un control local (factores locales). Los mecanismos de control de acción sistémica regulan el ritmo de activación de las BMU y la actividad funcional de las células que las integran. Son especialmente importantes la hormona paratiroidea y la vitamina D pero intervienen también las hormonas tiroideas, los esteroides sexuales, los glucocorticoides, la insulina y la hormona del crecimiento. La calcitonina aunque in vitro es capaz de modular la función de las células óseas parece que in vivo carece de importancia fisiológica. Algunas de estas hormonas tienen una acción directa sobre las células óseas; otras actúan de manera indirecta modulando la síntesis o la actividad de factores locales26. El control local del remodelado óseo se lleva a cabo a través de una serie de factores de crecimiento (insulina-like, transformantes de la familia ß, fibroblásticos, derivados de las plaquetas ) y citocinas (IL-1, IL-6, IL-11, factor de necrosis tumoral, factores estimuladores de colonias) de acción autocrina o paracrina10,11,14,15,26. Estos factores locales son producidos por las células óseas y las células medulares adyacentes (células hematopoyéticas, linfocitos, macrófagos). Los factores locales intervienen en el control de la actividad funcional de las células de las BMU y son clave para el acoplamiento entre osteoclastos y osteoblastos. Los células de linaje osteoblástico (lining cells) a través de la producción de factores locales (IL-6, IL-11) son capaces de activar a los osteoclastos y de esta manera contribuir al inicio de los ciclos de remodelado10,11. A su vez, ciertos factores liberados por los osteoclastos o por la matriz ósea bajo la acción de estas células son capaces de activar a los osteoblastos. Es probable que este fenómeno constituya el sustrato molecular para el acoplamiento entre la reabsorción y la formación dentro de los ciclos de remodelado. La mayoría de los datos que poseemos sobre la acción de los factores locales proceden de estudios in-vitro por lo que la importancia relativa de cada uno de estos factores in vivo se desconoce.
3.4 Reparación ósea (Fracturas)
El tejido óseo es el único capaz de repararse a sí mismo de manera completa a través de reactivar los procesos que tienen lugar durante su embriogénesis. Cuando de manera brusca, un hueso es sometido a fuerzas que superan su resistencia mecánica aparece una linea de fractura. En primer lugar, en esta zona, se produce un hematoma que es reabsorbido por macrófagos. A continuación, aparecen células formadoras de hueso, procedentes de ambos lados de la linea de fractura. Estas células establecen puentes de tejido óseo inmaduro, sin orientación espacial definida (callo de fractura), que unen entre si los extremos del hueso fracturado. En una fase posterior este hueso, a través de un proceso de modelado, es sustituido por otro, de tipo laminar, orientado según las líneas de fuerza que actuan sobre la zona4.
La fatiga mecánica puede causar microfracturas trabeculares que no modifican la morfología externa del hueso. Estas fracturas microscópicas se reparan a través de microcallos de fractura que muestran una dinámica similar a la de los grandes callos4.
[Índice] [Introducción] [Matriz] [Osteoblasto] [Osteoclasto] [Biomecanica] [Dinamica] [Bibliografía] |