
 Nº 737. Comunicación libre
Nº 737. Comunicación libre
|
Factores pronóstico del melanoma maligno Maria Concepción Garrido Ruiz[1], Jose Luis Rodriguez Peralto[2] |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
9;590;591;592;593;594;595;596;597;598;599;602;603;604;605;606;607;608;609;613;614;615;616;617;618;619;620;622;623;624;625;629;630;631;632;633;634;635;636;637;638;639;640;641;642;643;645;647;648;649;650;652;653;654;655;656;657;658;659;660;661;662;663;664;665;666;667;668;669;670;671;672;673;674;675;676;677;678;679;680;681;682;683;686;687;688;689;690;691;692;693;694;695;696;697;698;699;700;701;702;703;704;706;707;708;709;710;711;712;713;714;715;716;718;719;720;721;722;723;724;725;726;727;728;729;730;731;732;733;734;735;736;737;739;740;741;743;744;745;746;747;748;749;750;751;752;753;754;755;756;757;758;759;760;762;763;764;765;766;767;768;769;770;771;772;773;774;775;776;777;778;779;780;781;782;783;784;785;787;788;789;790;791;792;793;794;795;796;797;798;799;800;801;803;804;805;806;807;811;812;813;814;815;816;817;818;819;820;821;822;823;824;825;826;827;830;831;832;833;834;835;836;837;838;840;841;842;843;844;845;846;847;848;849;850;851;852;853;854;855;856;858;859;860;861;862;863;864;865;866;867;868;869;870;871;872;873;874;875;876;877;878;879;880;881;882;883;884;885;886;888;889;890;891;892;893;894;895;896;897;898;899;900;901;902;903;904;905;906;907;908;909;910;911;913;914;915;916;917;918;919;920;921;922;923;924;925;929;931;934;936;937;939;940;941;942;943;944;945;946;947;948;949;950;951;952;953;954;955;956;957;960;961;962;963;964;965;966;967;968;969;970;971;972;973;974;975;976;977;978;979;980;981;982;983;984;985;986;987;988;989;990;991;992;993;994;995;996;997;998;999;1000;1001;1002;1003;1004;1005;1006;1007;1008;1009;1010;1012;1013;1014;1015;1016;1017;1018;1019;1020;1021;1022;1023;1024;1025;1026;1027;1028;1029;1030;1031;1033;1034;1035;1036;1037;1038;1039;1040;1041;1042;1043;1044;1045;1046;1047;1048;1049;1050;1051;1052;1054;1055;1056;1057;1058;1059;1060;1061;1062;1063;1064;1065;1066;1067;1068;1069;1070;1071;1072;1073;1075;1076;1077;1078;1079;1080;1081;1082;1084;1085;1086;1087;1088;1089;1090;1091;1093;1094;1095;1096;1097;1098;1099;1100;1102;1103;1104;1105;1106;1107;1108;1109;1111;1112;1113;1114;1115;1116;1117;1118;1119;1120;1121;1122;1123;1124;1125;1126;1127;1128;1129;1130;1131;1132;1133;1134;1135;1136;1137;1138;1139;1140;1141;1142;1143;1144;1145;1146;1147;1148;1149;1150;1151;1152;1153;1154;1155;1156;1157;1158;1159;1160;1161;1162;1163;1164;1165;1166;1167;1168;1169;1170;1171;1172;1173;1174;1175;1176;1177;1178;1179;1180;1181;1182;1183;1184;1185;1186;1187;1188;1189;1190;1191;1192;1193;1194;1195;1196;1197;1198;1199;1200;1201;1202;1203;1204;1205;1206;1207;1208;1209;1210;1211;1212;1213;1214;1215;1216;1217;1218;1219;1220;1221;1222;1223;1224;1225;1226;1227;1228;1229;1230;1231;1232;1233;1234;1235;1236;1237;1238;1239;1240;1241;1242;1243;1244;1245;1246;1247;1248;1249;1250;1251;1252;1253;1254;1255;1256;1257;1258;1259;1260;1261;1262;1263;1264;1265;1266;1267;1268;1269;1270;1271;1272;1273;1274;1275;1276;1277;1278;1279;1280;1281;1282;1283;1284;1285;1286;1287;1288;1289;1290;1291;1292;1293;1294;1295;1296;1297;1298;1299;1300;1301;1302;1303;1304;1305;1306;1307;1308;1309;1310;1311;1312;1313;1314;1315;1316;1317;1318;1319;1320;1321;1322;1323;1324;1325;1326;1327;1328;1329;1330;1331;1332;1333;1334;1335;1336;1337;1338;1339;1340;1341;1342;1343;1344;1345;1346;1347;1348;1349;1350;1351;1352;1353;1354;1355;1356;1357;1358;1359;1360;1361;1362;1363;1364;1365;1366;1367;1368;1369;1370;1371;1372;1373;1374;1375;1376;1377;1378;1379;1380;1381;1382;1383;1384;1385;1386;1387;1388;1389;1390;1391;1392;1393;1394;1395;1396;1397;1398;1399;1400;1401;1402;1403;1404;1405;1406;1407;1408;1409;1410;1411;1412;1413;1414;1415;1416;1417;1418;1419;1420;1421;1422;1423;1424;1425;1426;1427;1428;1429;1430;1431;1432;1433;1434;1435;1436;1437;1438;1439;1440;1441;1442;1443;1444;1445;1446;1447;1448;1449;1450;1451;1452;1453;1454;1455;1456;1457;1458;1459;1460;1461;1462;1463;1464;1465;1466;1467;1468;1469;1470;1471;1472;1473;1474;1475;1476;1477;1478;1479;1480;1481;1482;1483;1484;1485;1486;1487;1488;1489;1490;1491;1492;1493;1494;1495;1496;1497;1498;1499;1500;1501;1502;1503;1504;1505;1506;1507;1508;1509;1510;1511;1512;1513;1514;1515;1516;1517;1518;1519;1520;1521;1522;1523;1524;1525;1526;1527;1528;1529;1530;1531;1532;1533;1534;1535;1536;1537;1538;1539;1540;1541;1542;1543;1544;1545;1546;1547;1548;1549;1550;1551;1552;1553;1554;1555;1556;1557;1558;1559;1560;1561;1562;1563;1564;1565;1566;1567;1568;1569;1570;1571;1572;1573;1574;1575;1576;1577;1578;1579;1580;1581;1582;1583;1584;1585;1586;1587;1588;1589;1590;1591;1592;1593;1594;1595;1596;1597;1598;1599;1600;1601;1602;1603;1604;1605;1606;1607;1608;1609;1610;1611;1612;1613;1614;1615;1616;1617;1618;1619;1620;1621;1622;1623;1624;1625;1626;1627;1628;1629;1630;1631;1632;1633;1634;1635;1636;1637;1638;1639;1640;1641;1642;1643;1644;1645;1646;1647;1648;1649;1650;1651;1652;1653;1654;1655;1656;1657;1658;1659;1660;1661;1662;1663;1664;1665;1666;1667;1668;1669;1670;1671;1672;1673;1674;1675;1676;1677;1678;1679;1680;1681;1682;1683;1684;1685;1686;1687;1688;1689;1690;1691;1692;1693;1694;1695;1696;1697;1698;1699;1700;1701;1702;1703;1704;1705;1706;1707;1708;1709;1710;1711;1712;1713;1714;1715;1716;1717;1718;1719;1720;1721;1722;1723;1724;1725;1726;1727;1728;1729;1730;1731;1732;1733;1734;1735;1736;1737;1738;1739;1740;1741;1742;1743;1744;1745;1746;1747;1748;1749;1750;1751;1752;1753;1754;1755;1756;1757;1758;1759;1760;1761;1762;1763;1764;1765;1766;1767;1768;1769;1770;1771;1772;1773;1774;1775;1776;1777;1778;1779;1780;1781;1782;1783;1784;1785;1786;1787;1788;1789;1790;1791;1792;1793;1794;1795;1796;1797;1798;1799;1800;1801;1802;1803;1804;1805;1806;1807;1808;1809;1810;1811;1812;1813;1814;1815;1816;1817;1818;1819;1820;1821;1822;1823;1824;1825;1826;1827;1828;1829;1830;1831;1832;1833;1834;1835;1836;1837;1838;1839;1840;1841;1842;1843;1844;1845;1846;1847;1848;1849;1850;1851;1852;1853;1854;1855;1856;1857;1858;1859;1860;1861;1862;1863;1864;1865;1866;1867;1868;1869;1870;1871;1872;1873;1874;1875;1876;1877;1878;1879;1880;1881;1882;1883;1884;1885;1886;1887;1888;1889;1890;1891;1892;1893;1894;1895;1896;1897;1898;1899;1900;1901;1902;1903;1904;1905;1906;1907;1908;1909;1910;1911;1912;1913;1914;1915;1916;1917;1918;1919;1920;1921;1922;1923;1924;1925;1926;1927;1928;1929;1930;1931;1932;1933;1934;1935;1936;1937;1938;1939;1940;1941;1942;1943;1944;1945;1946;1947;1948;1949;1950;1951;1952;1953;1954;1955;1956;1957;1958;1959;1960;1961;1962;1963;1964;1965;1966;1967;1968;1969;1970;1971;1972;1973;1974;1975;1976;1977;1978;1979;1980;1981;1982;1983;1984;1985;1986;1987;1988;1989;1990;1991;1992;1993;1994;1995;1996;1997;1998;1999;2000;2001;2002;2003;2004;2005;2006;2007;2008;2009;2010;2011;2012;2013;2014;2015;2016;2017;2018;2019;2020;2021;2022;2023;2024;2025;2026;2027;2028;2029;2030;2031;2032;2033;2034;2035;2036;2037;2038;2039;2040;2041;2042;2043;2044;2045;2046;2047;2048;2049;2050;2051;2052;2053;2054;2055;2056;2057;2058;2059;2060;2061;2062;2063;2064;2065;2066;2067;2068;2069;2070;2071;2072;2073;2074;2075;2076;2077;2078;2079;2080;2081;2082;2083;2084;2085;2086;2087;2088;2089;2090;2091;2092;2093;2094;2095;2096;2097;2098;2099;2100;2101;2102;2103;2104;2105;2106;2107;2108;2109;2110;2111;2112;2113;2114;2115;2116;2117;2118;2119;2120;2121;2122;2123;2124;2125;2126;2127;2128;2129;2130;2131;2132;2133;2134;2135;2136;2137;2138;2139;2140;2141;2142;2143;2144;2145;2146;2147;2148;2149;2150;2151;2152;2153;2154;2155;2156;2157;2158;2159;2160;2161;2162;2163;2164;2165;2166;2167;2168;2169;2170;2171;2172;2173;2174;2175;2176;2177;2178;2179;2180;2181;2182;2183;2184;2185;2186;2187;2188;2189;2190;2191;2192;2193;2194;2195;2196;2197;2198;2199;2200;2201;2202;2203;2204;2205;2206;2207;2208;2209;2210;2211;2212;2213;2214;2215;2216;2217;2218;2219;2220;2221;2222;2223;2224;2225;2226;2227;2228;2229;2230;2231;2232;2233;2234;2235;2236;2237;2238;2239;2240;2241;2242;2243;2244;2245;2246;2247;2248;2249;2250;2251;2252;2253;2254;2255;2256;2257;2258;2259;2260;2261;2262;2263;2264;2265;2266;2267;2268;2269;2270;2271;2272;2273;2274;2275;2276;2277;2278;2279;2280;2281;2282;2283;2284;2285;2286;2287;2288;2289;2290;2291;2292;2293;2294;2295;2296;2297;2298;22Introducción: El melanoma maligno cutáneo (MMC) es una neoplasia que se origina en los melanocitos de la piel, mucosas y en las células pigmentadas del globo ocular. Representa el 3-4% de las neoplasias cutáneas, aunque sin embargo es el responsable de la gran mayoría de las muertes debidos a cánceres cutáneos, originando el 65% de las muertes producidas por estos tumores, y en un contexto más general, a él se le atribuyen el 1% de la muerte por cáncer de cualquier etiología
Métodos: Se ha revisado extensamente la bibliografía, y se han obtenido datos a partir de nuestros propios estudios sobre melanomas (Hospital 12 de Octubre. Madrid) para establecer los diferentes factores pronóstico en relación con el melanoma maligno cutáneo .
Resultados: Los factores pronósticos en el melanoma son morfológicos, inmunohistoquímicos y clínicos, depende del momento evolutivo del tumor, y tendrán distinto significado.
Conclusión: En las últimas décadas, se ha alcanzado un mejor entendimiento de los factores pronóstico en el MMC, lo que ha permitido a su vez a los oncólogos a establecer el tratamiento más adecuado a cada paciente. Muchos de estos factores pronóstico están interrelacionados.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
En la antigua Grecia ya se conocía la enfermedad denominada cáncer, y sus avances habían progresado notablemente. La primera descripción de un melanoma aparece en los escritos de Hipócrates, en el siglo V antes de J.C.; asimismo, se ha detectado la enfermedad en varias momias incas precolombinas de aproximadamente la misma época. La primera publicación moderna sobre un paciente con la enfermedad, se debe a John Hunter en 1787. Inicialmente, la enfermedad fue denominada melanosis término acuñado por René Laennec en 1812. El término melanoma fue sugerido por primera vez por Robert Carswell en 1838. En 1907, William Sampson Handley describió las vías anatómicas de diseminación y su extensión linfática centrífuga. El melanoma supone el 3-4% de las neoplasias cutáneas, aunque sin embargo, es el responsable de la gran mayoría de las muertes debidas a cánceres cutáneos (1), originando el 65% de todas las muertes producidas por cánceres cutáneos y en un contexto más general, a él se le atribuyen el 1% de las muertes por cáncer de cualquier etiología (4). La incidencia de esta neoplasia ha ido creciendo de manera exponencial en la población mundial. La American Cancer Society (ACS) en Estados Unidos estima que alrededor de 59.940 nuevos casos de melanoma serán diagnosticados en este país durante 2007. El número de nuevos melanomas diagnosticados en EEUU está aumentando a expensas de hombres y mujeres de raza blanca, la incidencia aumenta alrededor del 6% por año desde 1973 hasta principios de los años 80. Desde 1980, el incremento se ralentiza: poco menos de 3% por año (1). En Europa, la incidencia del melanoma también ha aumentado espectacularmente, se calcula que en la última década su diagnóstico ha crecido aproximadamente un 60%. Así, en Suiza la incidencia desde los años 60 se ha multiplicado por cinco, y en España comparando la incidencia entre los años 80 y 90, ha aumentado cuatro veces (2). Es importante señalar que en países con baja frecuencia de melanoma, como los del Norte de Europa, también se ha incrementado la incidencia de forma ostensible. El melanoma afecta a todos los países del mundo, aunque históricamente, países como Chile y Australia han tenido las tasas de melanoma más elevadas (3). El melanoma es un tumor típicamente de adultos, suele aparecer en personas más jóvenes que la mayoría de los otros tipos de cáncer. La mitad de los melanomas se detectan en personas menores de 57 años de edad. Sin embargo los adolescentes también pueden desarrollar melanoma. Existe un pico diagnóstico en la cuarta década de la vida. Es más frecuente en hombres que en mujeres y, es excepcional en la infancia. Son muchos los factores implicados e la génesis del melanoma: la exposición solar, la piel clara (fototipos I y II), y especialmente las quemaduras solares antes de los 20 años, parecen ser los factores de riesgo más importantes. Es por ello que, evitar la exposición solar especialmente en las horas medias del día y durante la infancia juegue un papel primordial en la prevención del melanoma (3). El aumento de la incidencia del melanoma en los últimos años, podría estar en relación con un cambio en los patrones de exposición solar de la población junto con la disminución del espesor de la capa de ozono atmosférica. Algunos estudios demuestran una relación directamente proporcional entre la exposición a las radiaciones ultravioletas del sol y el desarrollo de nevus cutáneos, factor predisponerte para el posterior desarrollo de melanoma (5).
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Se ha revisado extensamente la bibliografía, y se han obtenido datos a partir de nuestros propios estudios sobre melanomas (Hospital 12 de Octubre. Madrid) para establecer los diferentes factores pronóstico en relación con el melanoma maligno cutáneo.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
1. Factores morfológicos: 1.a. Espesor tumoral (espesor de Breslow): Actualmente se acepta que éste es el factor pronóstico más importante. Mide la dimensión vertical máxima de infiltración desde la capa granulosa de la epidermis hasta la célula neoplásica más profunda que se observe. En algunas series la supervivencia a los 5 años para melanomas con poco espesor tumoral es del 100% (6); en lesiones con un espesor de 3,5 mm en otras series representan una mortalidad a los 10 años del 65% (7). En cualquier caso, se asume que el espesor de Breslow como factor pronóstico aislado sólo se puede usar de forma general, no es un predictor infalible de pronóstico de la enfermedad. Son muchas las cifras de Breslow que se han asignado para intentar separar grupos con distinto pronóstico (0,76 mm; 1,7 mm, 3 mm, 5mm), sin llegar a datos representativos. La American Joint Comité on Cancer (AJCC), establece unos porcentajes de supervivencia a los 10 años, en tumores diagnosticados en estadio clínico I, basados únicamente en el espesor de Breslow al diagnóstico: < 0,76 mm: 95% de supervivencia 0,76- 1,49 mm: 84% de supervivencia 1, 50-2, 49 mm: 69% de supervivencia 2, 50- 3,99 mm: 58% de supervivencia 4,00-7, 99 mm: 30% de supervivencia > 8,00 mm: 30% de supervivencia El pronóstico de los melanomas debe hacerse conjugando diferentes factores siendo uno de los más importantes el espesor tumoral o espesor de Breslow. 1.b. Nivel de Clark: El nivel de invasión tumoral está muy relacionado con el espesor tumoral máximo de una lesión y de ahí deriva su importancia pronóstica. La mayoría de las veces el melanoma comienza como una proliferación intraepidérmica de melanocitos malignos, que permanece confinada a la epidermis (nivel I de Clark) o dermis papilar superficial (nivel II de Clark), incluso décadas. Este estadio de desarrollo se denomina fase de crecimiento radial u horizontal, y en este punto la escisión quirúrgica es curativa. Según va progresando la enfermedad, las células neoplásicas infiltran y expanden la dermis papilar profunda (nivel III de Clark) y reticular (nivel IV de Clark) e incluso tejido celular subcutáneo (nivel V de Clark), adquiriendo capacidad metastásica. Este estadio de desarrollo se denomina fase de crecimiento vertical y aquí el pronóstico depende, no solo de la cirugía, sino también de distintos factores histológicos (8). Existe un subtipo histológico de melanoma, el melanoma nodular en el que no se identifican las fases de crecimiento radial y vertical, asumiendo que tiene capacidad metastásica desde el principio. Como factor pronóstico aislado, el nivel de Clark presenta algunas limitaciones. Puede existir variabilidad dentro de un mismo nivel de Clark (pe. Un melanoma polipoide de mayor espesor tumoral, nivel III de Clark tiene peor pronóstico que un melanoma no polipoide de menor espesor tumoral que también sea nivel III de Clark; este peor pronóstico se explica por la mayor cantidad y espesor de masa tumoral presente en la lesión polipoide). Otra limitación en la valoración del nivel de Clark es la subjetividad interobservador (9), especialmente la distinción entre los niveles II y III y, III y IV precoz de Clark. Un factor que favorece esta subjetividad en la valoración es el hecho de que la interfase dermis papilar-dermis reticular superficial, muchas veces es indistinguible anatomopatológicamente; este dato es especialmente significativo para las zonas acrales y mucosas (9). Existe un estudio en la literatura en el que se presenta una tasa de correlación interobservadores nivel I de Clark del 71,6% , del 66,7% para el nivel II; 69,1% para el nivel III y IV; y un 80% para el nivel V (10). 1.c.Fases de crecimiento: El melanoma presenta un peculiar patrón de crecimiento, que fue descrita por Clark y cols en los años 60 (11, 12), junto a los niveles de infiltración de Clark para el estadiaje de los melanomas. Esta peculiar forma de progresión tumoral se define de acuerdo a unos criterios establecidos en la literatura (13, 14):
Estas dos fases no siempre están presentes en todas las muestras de melanoma, pero el identificarlas proporcional una información esencial en su clasificación y futura evolución clínica (13). La mayoría de los trabajos de investigación en melanomas actualmente están orientados a buscar diferencias biológicas sustanciales entre estas dos fases de crecimiento y en particular, posibles cambios moleculares puntuales en las células neoplásicas en fase radial y en fase vertical que nos permitan predecir la evolución de las lesiones.( 13, 8). 1.d. Ulceración: Es un factor de mal pronóstico, especialmente importante cuando es mayor de 3 mm (15). Como factor pronóstico aislado, la ulceración es fácilmente reproducible en su valoración interobservador, pero se ha demostrado que su significado esta íntimamente ligado con el espesor tumoral, e incluso, algunos estudios demuestran su relación con el sexo del paciente y su localización anatómica (16). Por lo tanto, la ulceración no es un factor de riesgo independiente, aunque publicaciones recientes si demuestran que tiene una gran relevancia, junto con el espesor tumoral (17, 18). 1.e. Índice mitótico: Refleja la capacidad proliferativa de l tumor, es por lo tanto lógico que su relación sea inversamente proporcional con el pronóstico y la supervivencia (8). Sin embargo el primer problema que surge a la hora de cuantificar las mitosis es que no hay consenso claro en la literatura de cuál es la manera más objetiva. La tendencia actual es valorar la densidad mitótica por mm 2, en el corte histológico (19). Existen estudios que postulan que el índice mitótico es un factor pronóstico ligado al espesor tumoral (19), otro en cambio lo proponen como factor pronóstico independiente. 1.f. Células satélites La presencia de células neoplásicas localizadas a distancia de la masa tumoral primaria parece tener peor pronóstico como concepto histológico aislado (8). El problema está en saber cuántas células son necesarias para diagnosticar una satelitosis y a qué distancia mínima deben localizarse. Sin estos datos objetivos, la definición histológica se convierte en arbitraria (8). Clásicamente se consedera que los agregados de células neoplásicas deben ser de al menos 0,05 mmde diámetro y estra situados en la dermis, tejido celular subcutáneo o intravasculares, separads de la neoplasia primaria al menos 5cm (20, 21). Conceptualmente este término está intimamente relacionado con la insión vascular y las metástasis. 1.g. Respuesta linfocitaria acompañante El concepto de que la respuesta inmunitaria que desarrolla el huésped frente al tumor es importante y sugiere mejor pronóstico, es un hecho conocido (8), sin embargo, no existe ningún consenso objetivo en la literatura. Al hablar de respuesta inmunitaria, distintos autores se refieren al infiltrado linfocitario presente en la base del tumor, en los bordes laterales y dentro de la masa tumoral, hecho frecuente en la fase de crecimiento radial. Aunque existen numerosas controversias, la respuesta linfocitaria en la base tumoral sugiere mejor pronóstico (2). No obstante, su valor como factor pronóstico se pierde al ajustarlo con otros parámetros, especialmente con la fase de crecimiento y con el espesor tumoral, teniendo en cuenta la conocida relación inversa entre la respuesta inmunitaria y el espesor tumoral (2). 1.h. Subtipo histológico: Parece establecido que cualquier tipo de melanoma en función de su espesor de Breslow tiene el mismo pronóstico. Sin embargo se ha descrito una mejor evolución del lentigo maligno y un peor pronóstico de los melanomas lentiginosos acrales, independientemente de su espesor de Breslow.
1.i. Nevus asociado: El significado pronóstico de la presencia de nevus asociados a melanomas es controvertido (22). Se observan nevus asociados a melanomas en aproximadamente un tercio de los casos. Se ha sugerido un mejor pronóstico si existe esta asociación. 2. Factores inmuno histoquímicas 2.a. Metallothioneina La expresión de este marcador parece estar relacionada con un peor pronóstico (23, 24). 2.b. Osteonectina Se trata de una glicoproteina con múltiples funciones implicada entre otras cosas en la mineralización de los tejidos, supone un aumento en el riesgo de progresión y desarrollo de metástasis a distancia (25). 2.c. Integrinas Estas moléculas de adhesión están implicads en varios procesos de oncogenesis de forma todavía no muy establecida, pero parece que su acúmulo intracitoplasmático y en general el aumento de su expresión está relacionado con un peor pronóstico (26). 2.d. Proteina S-100 El anticuerpo contra la proteina S-100 fue el primer marcador inmunohistoquímico de uso rutinario en parafina, sobretodo como marcador de melanocitos, epitelio neural y células de Langerhans. Por tanto, la proteina S-100 es un buen marcador para melanocitospero desgraciadamente no permite distinguir las células neoplásicas de las no-neoplásicas. La proteína S-100 es el único marcador inmunohistoquímico intensamente positivo en los melanomas desmoplásicos y de células fusiformes (27). 2.e. HMB 45: Este anticuerpo se intento desarrollar inicialmente como marcador específico del melanoma aunque en poco tiempo se comprobó que se presentaba también en proliferaciones melanocíticas benignas. Y, los melanomas presentan habitualmente una tinción difusa de HMB-45, mientras que el nevus la pierde con la maduración del mismo en profundidad. Por lo tanto tampoco el HMB-45 es un tición de ayuda en las proliferaciones melanocíticas neopolásicas, aunque puede ayudar por su patrón de distribución (28) 2.f. Melan-A / MART-1: Es un antígeno de diferenciación melanocítica que se expresa como una proteína transmembranosa que inicialmente se detectó en melanocitos cutáneos normales, tejido retiniano y melanoma (29). Se expresa en lesiones melanocíticas benignas y malignas. Parece demostrado que Melan-A es un anticuerpo superior a HMB-45 en la detección de diferenciación melanocítica, y por tanto parece tener myor sensibilidad (30) que el HMB-45 en la detección de las metástasis del melanoma. Algunos autores describen la detección de altos niveles de expresión de melan-A como un factor de buen pronóstico (31). 2.g. Ki-67 Es un factor de proliferación celular. Se ha relacionado con un estadío clínico de mealnoma avanzado, junto con un factor de proliferación elevado como factores pronósticos independientes negativos en la evolución del melanoma (32). Este marcador es útil en la diferenciación de melanomas nevoides, en los que la distribución es difusa, de los nevus, en los que el Ki-67 se concentra en la zona superior de la dermis (32). 3. Factores clínicos a. Sexo. b. Edad. c. Localización de la lesión primaria. d. Nevus preexistente (ya comentado). e. Estadío clínico Las mujeres parecen tener mayor supervivencia que los hombres; la curva de supervivencia entre ambos géneros durante los primeros 2 años tras el diagnóstico es muy parecida, pero después varía, de modo que a los 5 años, la supervivencia de los hombres es sólo del 83%, frente al 90% de las mujeres. Es posible que esto se deba a la localización preferente en extremidades en la mujer, ya que se trata de una zona de pronóstico más favorable. Pacientes menores de 50 años tienen mejor pronóstico (supervivencia a 5 años del 90%) que los mayores de esa edad (del 84%). Esta diferencia se atribuye a varios factores, como espesor tumoral y perfiles hormonales: los pacientes mayores tienen lesiones de mayor espesor que los más jóvenes, y mayor porcentaje de MLA, de peor pronóstico medio. Por otra parte, en mujeres, el medio hormonal cambiante en la menopausia puede ser responsable del efecto adverso de la edad sobre el pronóstico. Localizaciones anatómicas de peor pronóstico son: cuero cabelludo, manuales y podálicas, mientras que el resto de extremidades parece ser una localización favorable. Las lesiones en la línea media, así como las situadas en partes acras de extremidades tanto superiores como inferiores, conllevan peor pronóstico independientemente del espesor de la lesión. El estadio clínico se establece siguiendo las recomendaciones de la American Joint Comittee on Cancer (1992) 4. Factores pronóstico en la enfermedad metastásica Según numerosos estudios, la supervivencia media de pacientes en estadio IV oscila de 4,7 a 11 meses, con una media de 8,5 meses; sin embargo, hay gran variabilidad individual, y se conocen supervivencias a largo plazo. La supervivencia estimada para estos pacientes a los 5 años es del 6-10%. Es importante su determinación, con objeto de orientar el tratamiento individual. a. Factores clínicos y anatomopatológicos: Los que predicen la supervivencia de forma independiente en estos pacientes son: -Número de puntos de metástasis. En pacientes con metástasis única, la supervivencia a 1 año fue del 36%, frente al 13% en pacientes con dos metástasis y al 0% en los que tenían 3 o más. -Duración de la remisión (inferior o mayor a 12 meses). -Localización de la enfermedad metastásica (visceral, no visceral, o ambas). La supervivencia a 1 año fue del 40% en los pacientes con metástasis no viscerales, del 11% en pacientes con metástasis viscerales, y del 8% en los que presentaban ambas. Asimismo, se cree que sexo, espesor, nivel de Clark del primario, localización inicial de las metástasis a distancia, número de puntos de metástasis, período libre de enfermedad y estadio previo de la misma, se asocian de forma significativa con la supervivencia. b. Parámetros analíticos: En pacientes en estadios III y IV, los siguientes factores son predictores significativos independientes de la supervivencia: - LDH sérica (su elevación, de mal pronóstico). -Albúmina sérica (su disminución, de mal pronóstico). -Recuento plaquetar. -Afectación visceral. -Sexo. c. Parámetros subjetivos: Calidad de vida. Se han realizado estudios sobre la influencia de la calidad de vida en la supervivencia, comprobándose que ciertos aspectos de la misma tienen poder predictivo independiente significativo, como son: -Índice de calidad de vida de Spitzer, que mide la misma en una escala según el médico. -Escala lineal análoga de autoevaluación (LASA), que mide la calidad de vida según el paciente, incluyendo el estado de ánimo y apetito. -Calidad de vida global. d. Factores genéticos: Se han estudiado como factores pronósticos la ploidía del ADN y la fracción de fase S en tejido tumoral. Se ha analizado también el nivel de expresión del gen nm23, que se cree que es un regulador principal del proceso metastásico, como marcador pronóstico en etapa metastásica. Se cree, aunque no está claro, que estos factores se relacionan con la supervivencia en estos pacientes
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
En las últimas décads, se ha alcanzado un mejor entendimiento de los factores pronóstico en el MMC, lo que ha permitido a su vez a los oncólogos a establecer el tratamiento más adecuado a cada paciente. Muchos de estos factores pronóstico están interrelacionados. Y, en un futuro no muy lejano, se prevé que los factores de biología y genética molecular nos proporcionen nuevos datos valiosos con un objetivo pronóstico, y porqué no terapéutico.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
4. Land H, Parada LF, Weinberg RA. Cellular oncogenes and multistep carcinogenesis. Science 1983; 222: 771-778. 5. Nowell PC. The clonal evolution of tumor cell populations. Science 1976; 194:23-28. 6. Clark WH, Elder DE, Guerry D, Epstein MN, Greene MH, van Horn M. A study of tumor progression. The precursor lesion of superficial spreading and nodular melanoma. Hum Pathol 1984; 15:1147-1165. 7. Breslow A. Thickness, cross-sectional-areas and depth of invasion in prognosis of cutaneous melanoma. Ann Surg 1970, 172: 902-904.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
- Fernando Terrasa Sagrista (02/05/2007 10:36:45)
- Dania Ledesma (02/06/2007 23:11:29)
- Javier Salamanca Santamaría (04/06/2007 17:43:54)
- CONCEPCION LARA (04/07/2007 11:15:44)
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Web mantenido y actualizado por el Servicio de informática uclm. Modificado: 16/06/2015 17:19:20
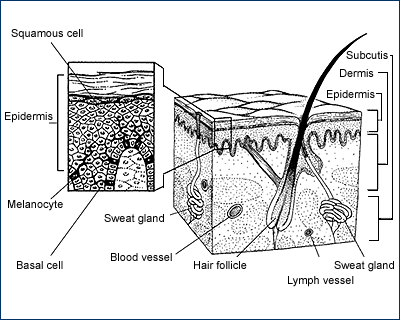 fiogf49gjkf0dEstructura normal de la piel">
fiogf49gjkf0dEstructura normal de la piel">
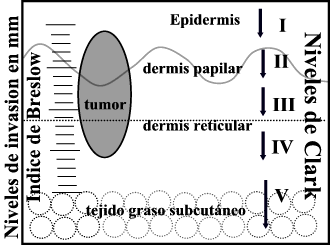 fiogf49gjkf0dNiveles de Clark">
fiogf49gjkf0dNiveles de Clark">